混合指示剂原理
混合指示剂原理
混合指示剂原理

实验原理
实验步骤
在某些酸碱滴定中,pH突跃范围很窄,使用一般的指示剂难以判断终点,此时可采用混合指示剂。混合指示剂利用颜色互补原理使终点颜色变化敏锐。
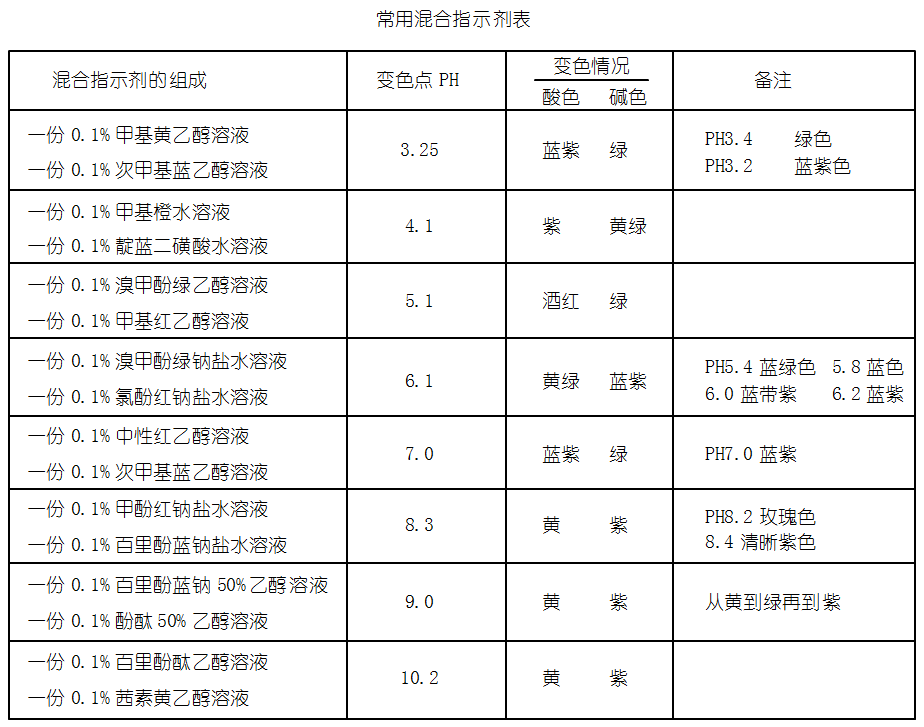
混合指示剂可分为两类,一类是在某种指示剂中加入一种惰性染料。例如由甲基橙和靛蓝组成的混合指示剂。靛蓝颜色不随pH改变而变化,只作为甲基橙的蓝色背景。在pH>4.4的溶液中,混合指示剂显绿色(黄与蓝配合),在pH<3.1的溶液中,混合指示剂显紫色(红与蓝配合),在pH=4的溶液中,混合指示剂显浅灰色(几乎无色),终点颜色变化非常敏锐。
另一类是由两种或两种以上的指示剂混合而成。例如溴甲酚绿(pKa4.9,黄→蓝)和甲基红(pKa5.2, 红→黄),按3:1混合后,使溶液在酸性条件下显酒红色(黄+红),碱性条件下显绿色(蓝+黄),而在pH5.1时二者颜色发生互补,产生灰色,使颜色在此时发生突变,变色十分敏锐,常常用于用Na2CO2为基准物质标定盐酸标准溶液的浓度。
实验交流
共享应用
-
浏览量 3810
-
点赞数 0
-
收藏数 0
课程评分
0
课程回复
-
评论数 0

