电极电势的产生
电极电势的产生
电极电势的产生

实验原理
实验步骤
1. 由于金属晶体是由金属原子、金属离子和自由电子所组成,当我们把金属插入含有该金属盐的溶液时(如将锌棒插入硫酸锌溶液中),初看起来似乎不起什么变化。实际上会同时发生两种相反的过程。一方面,受到极性水分子的作用以及本身的热运动,金属晶格中的金属离子Mn+有进入溶液成为水合离子而把电子留在金属表面的倾向,金属越活泼,金属离子浓度越小,这种倾向越大。另一方面,溶液中的金属离子Mn+也有从金属表面获得电子而沉积在金属表面上的倾向,金属越不活泼,溶液中金属离子浓度越大,这种沉积倾向越大。在一定条件下,当金属溶解的速率与金属离子沉积的速率相等时,就建立了如下的动态平衡:
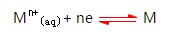
2. 当金属溶解的倾向大于金属离子沉积的倾向,则达到平衡时,金属表面带负电,靠近金属的溶液带正电。这样,在金属表面和溶液的界面处就形成了一个带相反电荷的双电层(electron double layer)。相反,若金属离子沉积的倾向大于金属溶解的倾向,平衡时,金属表面带正电,靠近金属的溶液带负电,形成了双电层结构。
3. 无论形成上述的哪一种双电层, 双电层的厚度虽然很小(约为10-8cm数量级),但金属和溶液之间都可产生电势差。这种在金属和它的盐溶液之间因形成双电层而产生的电势差叫做金属的平衡电极电势,简称电极电势(electrode potential),以符号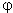 Mn+/M表示。单位为V(伏)。如锌的电极电势
Mn+/M表示。单位为V(伏)。如锌的电极电势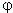 Zn2+/Zn用表示,铜的电极电势
Zn2+/Zn用表示,铜的电极电势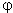 Cu2+/Cu用表示。电极电势大小主要取决于电极的本性,并受温度、介质和离子浓度等因素影响。
Cu2+/Cu用表示。电极电势大小主要取决于电极的本性,并受温度、介质和离子浓度等因素影响。
实验交流
共享应用
-
浏览量 6406
-
点赞数 0
-
收藏数 0
课程评分
0
课程回复
-
评论数 0

